抗體(Antibody)這個詞首次出現在保羅·埃爾利希1891年10月公布的《免疫力的試驗性研究》這篇文章中,德語的抗體“Antik?rper”出現在該文章的結論部分。其中指出了“如果兩種物質導致兩種不同抗體的產生,那么這兩種物質必然是不同的”。然而這一術語并沒有立即被接受,還有被建議使用的其它幾個術語,如:免疫體(Immunk?rper)、介體受體(Amboceptor)、介體(Zwischenk?rper)、物質敏感體(substance sensibilisatrice)、連接體(copula)、德氏體(Desmon)、白細胞素(philocytase)、介體固定體(fixateur)以及免疫素(Immunisin)等。抗體和抗毒素(Antitoxin)字面結構相似,概念則和免疫體(Immunk?rper)類似。
根據E. Padlan公布的抗體結構圖,朱利·安沃斯-安德烈*為斯克里普斯研究所佛羅里達分部創作了雕塑《西方天使》(2008年)塑像仿照列奧納多·達·芬奇的維特魯威人,將抗體放置到一個圓環的中間,寓意其對于人類的重要意義。
針對抗體的研究始于1890年,埃米爾·阿道夫·馮·貝林及北里柴三郎首次描述了抗體對白喉及破傷風痙攣毒素的抵抗作用。他們兩人將體液免疫理論往前推進了一步,提出了血清中存在一種可以與外來抗原相反應的某種介質的假設。保羅·埃爾利希受到了他們的這一想法的啟發,于1897年提出了抗體與抗原互動的側鏈理論假說。他假設道,在細胞的表面存在能和特定毒素發生一把鑰匙對應一把鎖類似的特異結合作用的感受器,而結合反應則會進一步導致相關抗體的生產。其他研究人員在之后的研究中認為,抗體可以在血液中穩定獨立存在。在1904年,奧姆羅斯·萊特進一步提出通過可溶性抗體在細菌的表面包裹標識,使其成為吞噬作用的目標,并最終被消滅。這一過程被他命名為調理作用。
到了二十世紀二十年代,邁克爾·海德堡和奧斯瓦爾德·埃弗里觀察到抗原可以被抗體所凝結,并進一步發現抗體是一種蛋白質。在三十年代,約翰·馬拉克對抗原-抗體結合活動的生物化學性質做了更詳盡的實驗。接下來的一次重大突破發生在四十年代,萊納斯·鮑林通過抗體抗原的互動能力取決于各自的形狀而不是其化學成分,證明了埃爾利希所提出的一把鑰匙配一把鎖的免疫學理論。1948年,阿斯特麗德·法戈瑞奧司發現B細胞的其中一種形式漿細胞就是負責生產抗體的工廠。
此后,研究工作的重點轉向了識別抗體蛋白質結構中各部分的作用。二十世紀六十年代,杰拉爾德·埃德爾曼和約瑟夫·蓋里發現了抗體的輕鏈,并且發現這和1845年由亨利·本冊·瓊斯所發現的本周氏蛋白質是同一種物質,這是一項重大的突破。緊接著,埃德爾曼在進一步發現抗體中的重鏈和輕鏈是由雙硫鍵連接在一起的。與此同時,羅德尼·羅伯特·波特識別出了免疫球蛋白的抗體結合區(Fab)及抗體尾部的可結晶區。根據這些發現,科學家們對免疫球蛋白的結構進行了推測,并描述了IgG蛋白質的完整氨基酸序列。
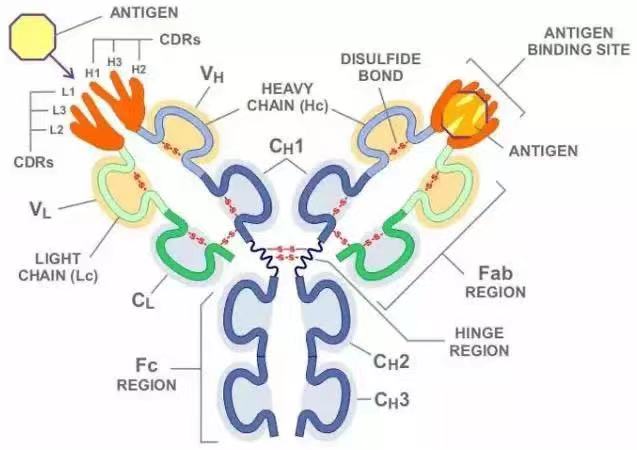
抗體,又稱為免疫球蛋白(immunoglobulin,簡稱Ig),是一種主要由漿細胞分泌,被免疫系統用來鑒別與中和外來物質如細菌、病毒等病原體的大型Y形蛋白質,僅被發現存在于脊椎動物的血液等體液中,及其B細胞的細胞膜表面。抗體能通過其可變區唯一識別特定外來物的一個獨特特征,該外來目標被稱為抗原(Antigen)。蛋白上Y形的其中兩個分叉頂端都有一被稱為互補位(抗原結合位)的鎖狀結構,該結構僅針對一種特定的抗原表位。這就像一把鑰匙只能開一把鎖一般,使得一種抗體僅能和其中一種抗原相結合。 抗體和抗原的結合完全依靠非共價鍵的相互作用,這些非共價鍵的相互作用包括氫鍵、范德華力、電荷作用和疏水作用。這些相互作用可以發生在側鏈或者多肽主干之間。正因這種特異性的結合機制,抗體可以“標記”外來微生物以及受感染的細胞,以誘導其他免疫機制對其進行攻擊,又或直接中和其目標,例如通過與入侵和生存至關重要的部分相結合而阻斷微生物的感染能力等。針對不同的抗原,抗體的結合可能阻斷致病的生化過程,或者召喚巨噬細胞消滅外來物質。而抗體能夠與免疫系統的其它部分交互的能力,是通過其Fc區底部所保留的一個糖基化座實現的。體液免疫系統的主要功能便是制造抗體。抗體也可以與血清中的補體一起直接破壞外來目標。
抗體是一種高分子球狀血液蛋白質,重量約為150kDa。由于在部分氨基酸殘基中含有糖鏈,抗體也是一種糖蛋白。能發揮功能的基本單位是一個免疫球蛋白單體。在分泌形態的抗體中包括:二聚體IgA、真骨附類魚的四聚體IgM以及哺乳動物的五聚體IgM。
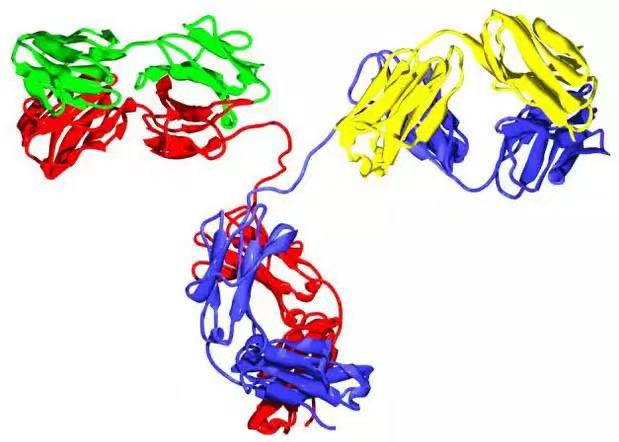
抗體的單體是一個Y形的分子,有4條多肽鏈組成。其中包括兩條相同的重鏈,以及兩條相同的輕鏈,之間由雙硫鍵連接在一起。每一條鏈均由稱為免疫球蛋白結構域的多個結構域所組成。每一個結構域大約包含70至110個氨基酸,并根據大小和功能分門別類。例如可變域IgV以及恒定域IgC。它們的折疊方式很特別:通過兩次β折疊將另一條鏈卷入其中形成三明治狀,互相之間通過半胱氨酸和其它帶電荷氨基酸緊密結合。
哺乳動物的免疫球蛋白重鏈有5種,分別用希臘字母記為:α、δ、ε、γ以及μ。根據重鏈類型的不同,抗體被分為不同的種型,它們被發現依序分別存在于抗體IgA、IgD、IgE、IgG以及IgM中。不同的重鏈其大小和組成各不相同:α和γ大約有450個氨基酸組成,而μ和ε大約有550個氨基酸組成。
1. 抗原結合區(Fab)
2. 抗原結晶區(Fc)
3. 藍色的重鏈有一個可變區(VH),緊隨其后的一個恒定區(CH1),一個樞紐區,以及另兩個恒定區(CH2 and CH3)組成
4. 綠色的輕鏈包含一個可變區(VL)以及一個恒定區(CL)
5. 抗原結合點
6. 樞紐區.
在鳥類的血液和蛋清中,還發現了被稱為IgY的血清抗體種型。這種抗體種型和哺乳動物的IgG有很大的區別。然而在一些舊資料,甚至是生命科學商業產品的網站上,仍然稱之為IgG。這是錯誤的,并且容易引起混淆。
每一條重鏈有兩個區域:恒定區與可變區。同種型的抗體,其恒定區都是一樣的,但不同種型之間該區域是不相同的。例如:γ、α以及δ型重鏈由三個免疫球蛋白結構域串聯而成,并且還有一個用于增加彈性的鉸鏈區;而μ及ε型重鏈則包括四個免疫球蛋白結構域。不同B細胞所生產抗體的重鏈可變區是不同的,但是同一個B細胞及其克隆體所生產的不同種型抗體的可變區則是完全相同的。重鏈的可變區由一個結構域組成,包含大110個氨基酸。
免疫球蛋白輕鏈由大約211至217個氨基酸組成,分為兩個結構域,分別是恒定區和可變區。哺乳動物的輕鏈有兩種,分別命名為λ(lambda)和κ(kappa)。每一個抗體的兩個輕鏈的恒定區永遠是完全相同的,例如對于哺乳動物而言,同一個抗體要么是λ型,要么是κ,不會同時存在。在如軟骨魚綱(鯊魚)及真骨下綱的低級脊椎動物中,還可發現其它類型的輕鏈,如ι(iota)型。
抗體的某些部分具有獨特的功能。比如說Y形的臂區,包含了兩個可以結合抗原的位點,是識別外來物的關鍵所在。該區域被稱為Fab區,即抗原結合區段(fragment, antigen binding)。無論是重鏈還是輕鏈,抗原結合區段均包括一個可變區與一個恒定區,其中可變區的互補位成型于抗體單體氨基酸鏈的末端。可變區又被稱為Fv區,是與抗體結合的最關鍵區域,無論是輕鏈還是重鏈都包含該區域。實際上可變區的變化并非隨機或者均勻散布的。更具體的說,這些變化分布在三個可變的β折疊-轉角上,該區域被稱為互補決定區(Complementarity Determining Region,CDR),也叫做高變區。在免疫網絡理論中,每個抗體的互補決定區又被稱為獨特型或者基因型。適應性免疫系統的適應過程,就是依靠有各個獨特型之間的互動來進行調整的。
------------------------------------------------
參閱文獻:
1.Rhoades RA, Pflanzer RG (2002). Human Physiology (4th ed.). Thomson Learning. p. 584. ISBN 0-534-42174-1.
2.Charles Janeway (2001). Immunobiology. (5th ed.). Garland Publishing. ISBN 0-8153-3642-X. (electronic full text via NCBI Bookshelf)
3. Pier GB, Lyczak JB, Wetzler LM (2004). Immunology, Infection, and Immunity. ASM Press. ISBN 1-55581-246-5.
4.Borghesi L, Milcarek C (2006). "From B cell to plasma cell: regulation of V(D)J recombination and antibody secretion". Immunol. Res. 36 (1–3): 27–32. doi:10.1385/IR:36:1:27. PMID 17337763
5.參考資料:https://en.wikipedia.org/wiki/Antibody


